上海宇玫博生物科技有限公司品牌商
9 年
手机商铺
- NaN
- 0
- 1
- 2
- 1
上海宇玫博生物科技有限公司
入驻年限:9 年
- 联系人:
宇玫博
- 所在地区:
上海 浦东新区
- 业务范围:
技术服务、耗材、实验室仪器 / 设备、细胞库 / 细胞培养、论文服务、试剂、原辅料包材
- 经营模式:
生产厂商 经销商 科研机构
公司新闻/正文
IF=20.3 | Umibio外泌体专用无血清培养基助力客户牙周组织再生研究!
227 人阅读发布时间:2026-01-23 16:43

近期,来自广州海洋实验室的陈凯教授,昆明医科大学口腔医学院的杨禾丰教授和胡江天教授团队在Bioactive Materials杂志发表了题为“miR-423-5p-enriched small extracellular vesicles drive periodontal regeneration via Sfrp2+ cell expansion”的科研论文,IF=20.3。

研究背景:
牙周缺损(periodontal defect)是牙周炎引发的成年人牙齿脱落的主要原因,严重损害身体健康和生活质量。现有的治疗方法(菌斑清除、药物治疗、手术)仅能控制病情,无法实现牙骨质、牙周韧带和牙槽骨的协同功能性再生。小细胞外囊泡(sEVs)作为细胞间通讯载体,可通过调控微环境促进组织再生,但因其成分复杂导致治疗效果不稳定,限制了临床转化。MicroRNA 是sEVs 中富集的关键调节因子,可通过靶向下游基因来影响疾病进展和组织再生,作为sEVs的生物活性成分,miRNA可调节关键细胞过程(增殖、分化和凋亡)。近期的研究表明,工程化囊泡以递送功能性miRNA或抑制有害miRNA来调节受体细胞功能,是干预疾病进展和增强组织修复的有效策略。本研究旨在识别sEVs中的关键再生成分,揭示工程化sEVs有作为牙周炎个性化再生疗法的潜力。
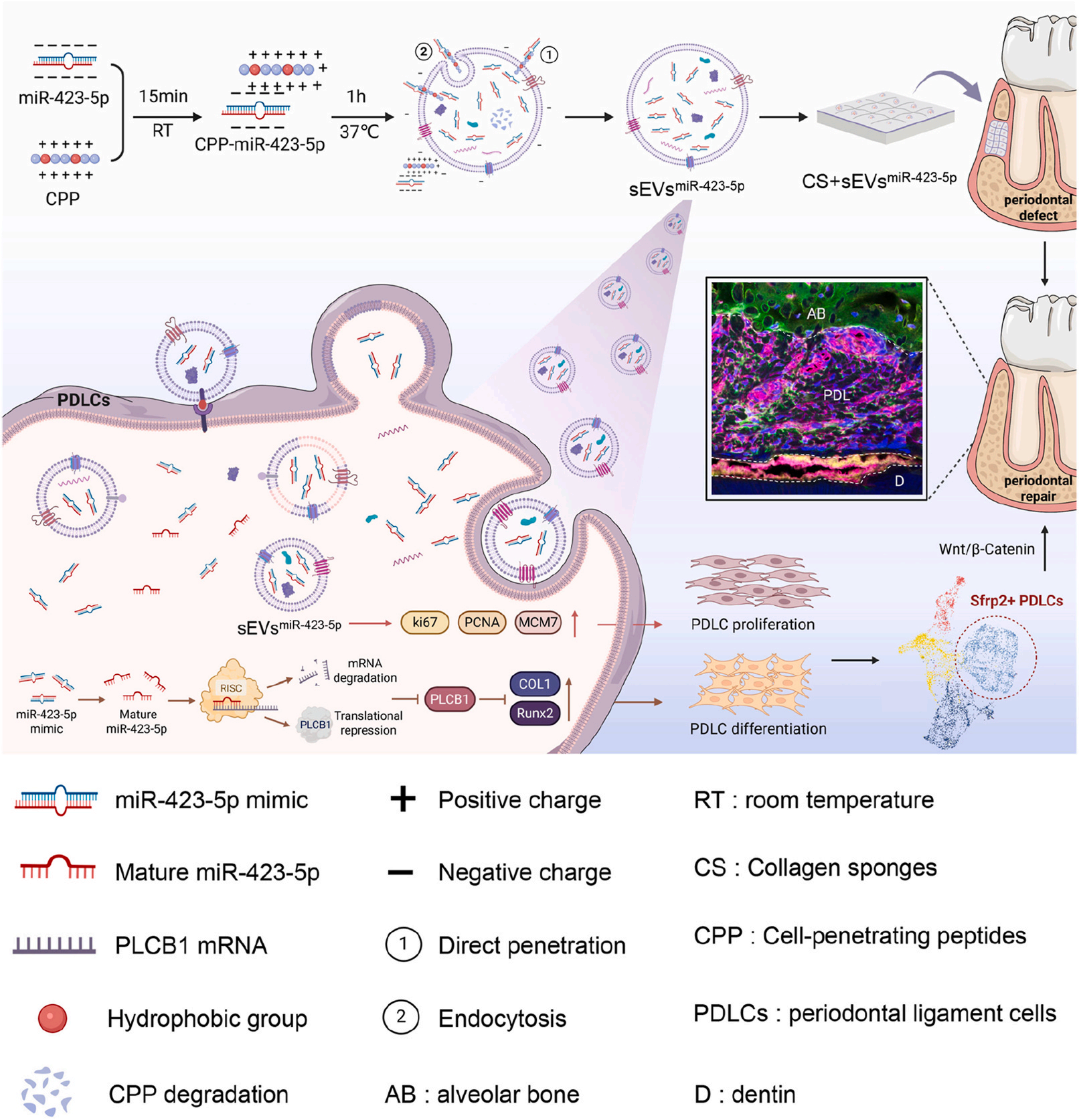
研究成果及意义:
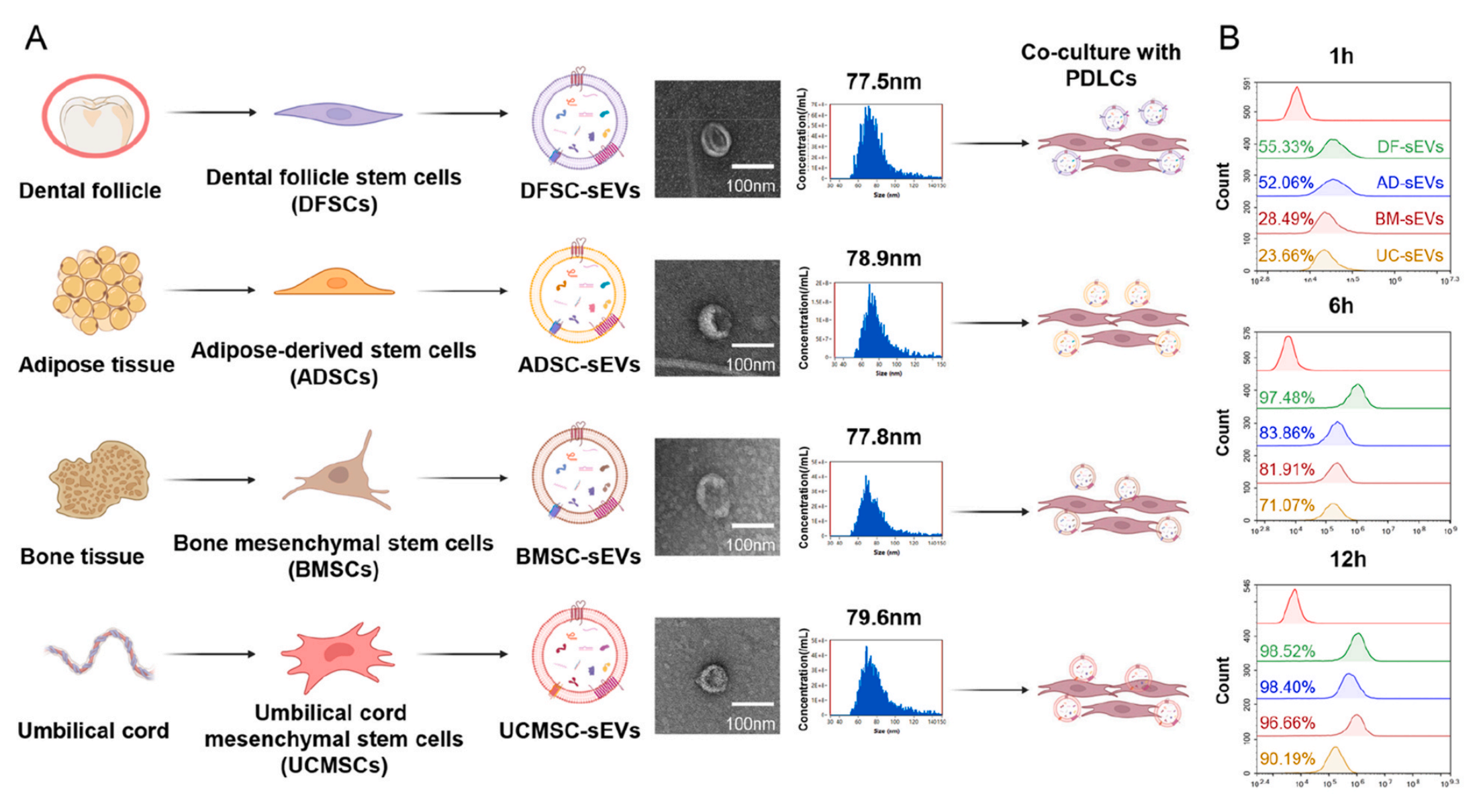
在本研究中,作者首先分离了 4 种干细胞(DFSCs/ADSCs/BMSCs/UCMSCs)的sEVs,并检测了牙周膜细胞(PDLCs)摄取效率及成骨效应。结果发现DFSC-sEVs 被PDLCs摄取最快,6h摄取率达81.91%。功能实验证实,DFSC-sEVs增强了PDLCs的ALP活性和矿化结节形成,具有PDLCs亲和力和骨诱导潜能。接着作者利用miRNA测序和生物信息学分析,作者确定了前20个最丰富的miRNAs,其中miR-148a-3p、miR-423-5p、miR-100-5p和miR-125b-5p的表达水平高于亲本DFSCs,ARS和ALP染色结果显示,miR-423-5p在DFSC-sEVs中表达水平最高,且有最显著的增强成骨分化效果。这些结果表明miR-423-5p 是DFSC-sEVs中促进PDLCs成骨分化的关键因子。为了确定miR-423-5P的下游靶点,作者通过miRTarBase、miRWalk和TargetScan预测得到了63个高置信度候选基因,它们主要参与细胞运输和功能调节等生物学过程。其中4个基因(DAAM2、PRKACA、DVL3和PLCB1)富含在Wnt信号通路中。双荧光素酶报告基因实验和功能实验进一步证实了miR-423-5P和PLCB1特异性结合,miR-423-5p抑制PLCB1是促进PDLCs成骨分化的关键机制。随后作者使用细胞穿膜肽(CPP)的方法构建了富含miR-423-5p的工程化小细胞外囊泡sEVsmiR−423−5p,鉴定结果表明与未修饰的SEVs相比,sEVsmiR−423−5p的形态、大小、表面标志蛋白和Zeta电位相似,miR-423-5p的水平提升10万倍,并且保持了sEVs的结构完整性和稳定性。为了观察PDLCs摄取sEVsmiR−423−5p的情况,作者将荧光标记的sEVsmiR−423−5p与PDLCs共培养,结果发现sEVsmiR−423−5p能被牙周膜细胞高效摄取并稳定释放miR-423-5p,且不改变其他miRNA的表达。为了评估sEVsmiR−423−5p在PDLC中的细胞内稳定性,作者进行了体外实验,结果发现sEVsmiR−423−5p能将miR-423–5p高效地传递到PDLCs 中,并被整合入Ago2,形成RISC。后续增殖检测显示,sEVsmiR−423−5p具有促进PDLCs增殖的能力,其中PCNA、MCM7和Ki67蛋白表达显著上调。骨生成诱导后,sEVsmiR−423−5p组ALP活性增强,Runx2和COL1基因表达上调。在分子机制上,sEVsmiR−423−5p能有效下调其靶蛋白PLCB1的表达,并同时激活Wnt/β-catenin通路。这些结果表明sEVsmiR−423−5p不仅保留了天然sEVs的增殖能力,而且显著增强了成骨活性。为了验证sEVsmiR−423−5p的生物相容性及安全性,作者构建了大鼠牙周缺损模型并将负载sEVsmiR−423−5p的胶原海绵植入体内牙周缺损处,结果发现胶原海绵作为生物相容性优良的载体,实现了囊泡的局部持续释放,72小时内可以完全释放。组织学分析显示没有病理变化,也没有γH2A.X表达,表明全身毒性极小。牙周再生需要整合牙骨质、牙周韧带和牙槽骨的修复,而不仅仅是骨再生。植入6周后,再生骨显得致密、光滑、连续,与周围完整骨非常相似,骨密度显着高于对照组。这些实验结果表明sEVsmiR−423−5p增强了大鼠牙周缺损的早期成骨,并促进了牙本质与新生骨之间牙周韧带样纤维的生成。最后作者进行了单细胞RNA测序分析,结果发现成纤维细胞构成了牙周组织中的主要细胞群,并在其发育和再生过程中起着核心作用。为了识别sEVsmiR−423−5p主要靶向的特定成纤维细胞亚群,作者进行了基因表达聚类分析(GO)和功能富集分析(KEGG),结果发现sEVsmiR−423−5p可显著扩增牙周缺损部位的Sfrp2+成骨成纤维细胞,Sfrp2+成纤维细胞中的基因主要参与含胶原的细胞外基质组织、细胞外结构组织、细胞生长和骨发育的调节以及Wnt信号传导的调节。Wnt信号传导是调节骨形成的经典途径,在体外已经证明 sEVsmiR−423−5p通过沉默PLCB1 从而激活经典的Wnt/β-catenin信号通路来促进 PDLCs 的成骨分化。免疫荧光染色结果表明Sfrp2与β-catenin在缺损牙本质表面共定位,形成类似天然牙周组织的三明治结构,为再生效果提供了关键结构支撑。
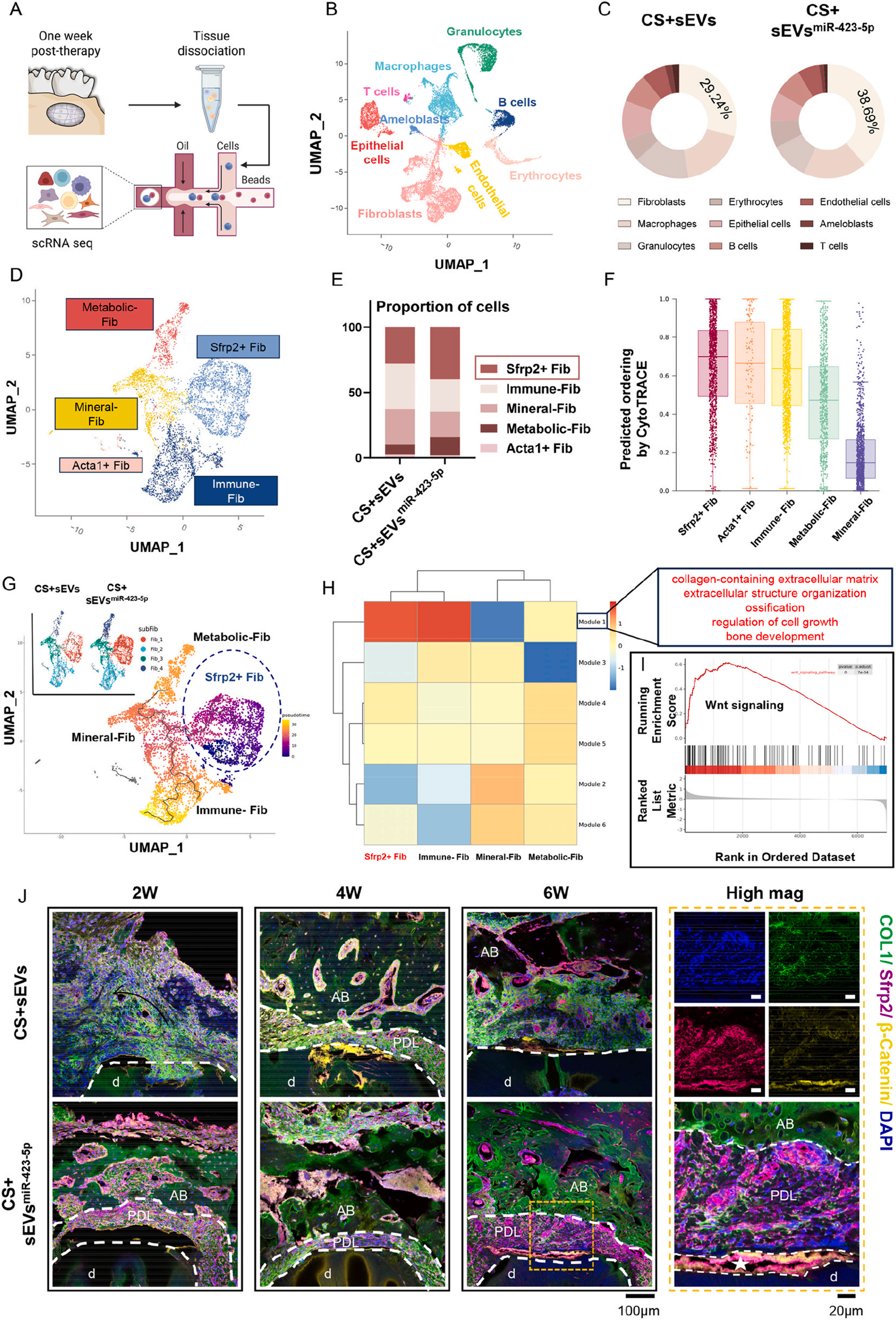
综上所述,作者认为miR-423-5p是促进PDLCs增殖和成骨分化的关键sEVs来源的调节因子。作者构建的miR-423-5p富集型工程化囊泡sEVsmiR−423−5p中miRNA负载量较天然sEVs提升了10万倍,该工程化囊泡不仅能将miRNA精准、高效地递送至牙周靶细胞,更能通过靶向抑制PLCB1基因,激活Wnt/β-catenin信号通路,从而特异性扩增具有高干性的Sfrp2+成纤维细胞。这项研究首次明确miR-423-5p在牙周再生中的关键作用,提供了高效、稳定的工程化sEVs构建策略,为牙周炎及其他组织缺损的无细胞再生治疗提供了新的理论依据和技术平台。

该研究中使用本公司的外泌体专用无血清培养基(货号:UR51102)对DFSCs, ADSCs, BMSCs, 和 UCMSCs细胞进行了培养,在排除外源血清外泌体干扰的情况下保证了细胞短期内的正常生长和外泌体的正常分泌,为接下来外泌体的提取纯化实验提供了高质量的细胞上清。结果符合各检测指标要求,满足了客户下游实验需求。随后作者使用细胞穿膜肽(CPP)的方法构建了富含miR-423-5p的工程化小细胞外囊泡sEVsmiR−423−5p,鉴定结果表明与未修饰的sEVs相比,sEVsmiR−423−5p的形态、大小、表面标志蛋白和Zeta电位相似,miR-423-5p的水平提升10万倍,并且保持了sEVs的结构完整性和稳定性。
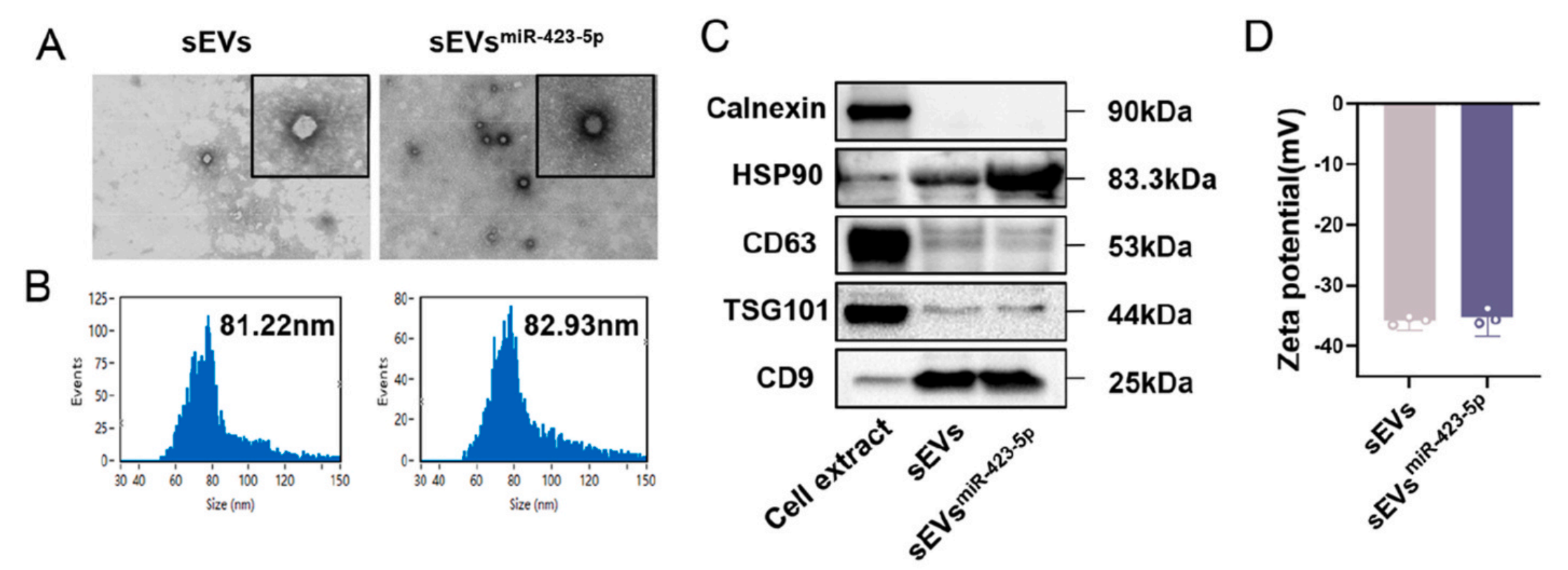
参考文献:miR-423-5p-enriched small extracellular vesicles drive periodontal regeneration via Sfrp2+ cell expansion. Bioactive Materials.2025 Nov 29;58:19-32.
相关产品:UR51102
获取全文请扫描下方二维码: