上海宇玫博生物科技有限公司品牌商
9 年
手机商铺
- NaN
- 0
- 1
- 2
- 1
上海宇玫博生物科技有限公司
入驻年限:9 年
- 联系人:
宇玫博
- 所在地区:
上海 浦东新区
- 业务范围:
技术服务、耗材、实验室仪器 / 设备、细胞库 / 细胞培养、论文服务、试剂、原辅料包材
- 经营模式:
生产厂商 经销商 科研机构
公司新闻/正文
IF=12.5 | Umibio多款核心产品助力客户创伤性脑损伤后急性肾损伤研究!
134 人阅读发布时间:2026-03-17 16:10

近期,来自天津医科大学的闫华教授、张国斌教授和徐立霞教授团队在Science Advances杂志发表了题为“Brain-derived extracellular vesicles circUsp32 polarized macrophages causing acute kidney injury after traumatic brain injury”的科研论文,IF=12.5。

研究背景:
创伤性脑损伤 (TBI ) 是全球主要致死和致残原因,除中枢损伤外,还会引发全身病理改变,急性肾损伤(AKI)是其常见并发症,临床发生率为10%-15%。TBI 可诱导 AKI,而肾损伤也会通过毒素蓄积等诱发神经炎症和认知障碍,但具体分子机制尚未明确。细胞外囊泡(EVs)是器官间通讯的重要介质,TBI可诱导脑释放病理性EVs,穿越血脑屏障进入循环引发多器官功能障碍;环状RNA(circRNAs)在免疫调控中起关键作用,但TBI-EVs中的circRNAs 对 AKI 的调控作用尚未被阐明。巨噬细胞的促炎/抗炎极化是 AKI 发生的核心病理机制,多种因子可调控该过程,但TBI-EVs 如何调控巨噬细胞极化进而诱发AKI 仍不清楚。本文旨在研究TBI引发AKI的分子作用机制,为脑损伤诱导的AKI和脑-肾交互提供关键的机制见解。
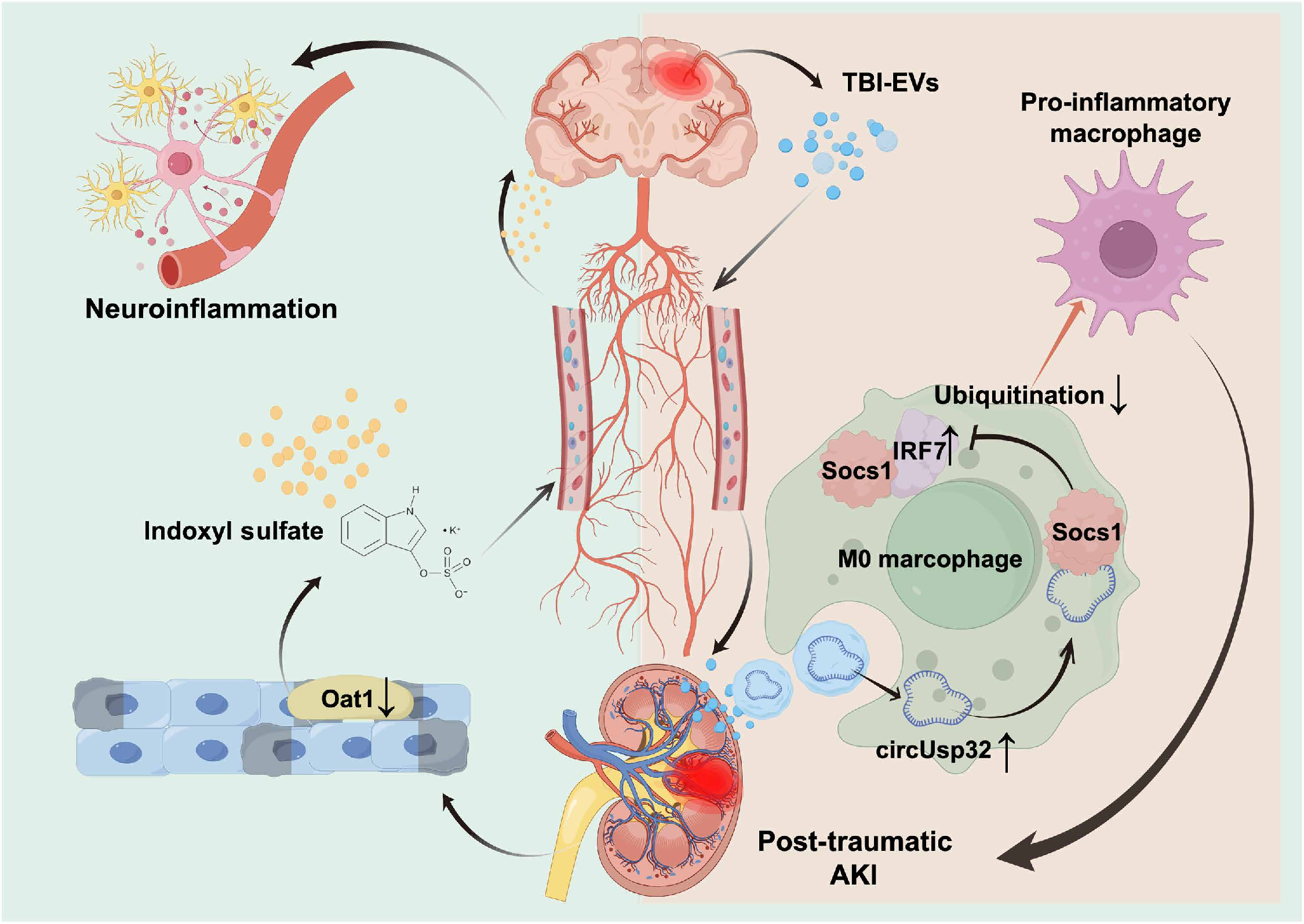
研究成果及意义:
在本研究中,作者首先构建了TBI小鼠模型并进行了肾功能评估和肾组织病理学分析,结果发现TBI后24h时血尿素氮(BUN)、血清肌酐(Scr)、肾损伤分子(KIM-1)和NGAL等AKI标志物均达峰值;肾组织病理学分析显示肾小管损伤、细胞凋亡最显著,促炎细胞因子(TNF-α、IL-6、IL-1β)表达最高。这些结果表明,AKI在TBI后24小时表现最为明显。随后作者在TBI后24小时从小鼠脑组织中分离出脑损伤后的TBI-EVs并进行了鉴定,结果显示TBI-EVs呈茶托型结构,粒径大小在200nm以下,标志蛋白CD9、CD81、TSG101表达,而Calnexin在TBI-EVS中不表达;此外,TBI-EVS中GFAP的存在证实了它们来自脑组织。尾静脉注射后发现TBI-EVs可在小鼠心、肺、肝、肾、脾中富集,肾脏中12h 达峰,48h开始下降,证实其可靶向肾脏发挥作用。由于巨噬细胞极化在AKI过程中发挥了重要作用,作者推测TBI-EVs可以促进巨噬细胞极化,随后进行了双重免疫荧光染色和流式细胞分析,结果发现TBI-EVs可显著升高 AKI 标志物,诱发肾小管损伤和细胞凋亡,同时使肾脏中促炎巨噬细胞(iNOS+)比例升至33.7%,抗炎巨噬细胞(CD206+)比例显著降低,证实TBI-EVs是介导TBI后AKI的关键介质。随后作者进行了RNA测序,对比TBI-EVs和Sham-EVs的circRNA表达谱发现circUsp32(mmu_circ_0000303)是上调最显著的circRNA,经 qRT-PCR 和Sanger测序验证CircUsp32位于第11号染色体上的Usp32基因的四个外显子。KEGG分析显示circUsp32富集于HIF-1、JAK-STAT、TLR 等免疫相关通路。接着作者进行了体外实验,结果表明TBI-EVs能被RAW264.7巨噬细胞摄取并上调其circUsp32表达。circUsp32在翻译后水平调控TLR通路核心分子IRF7,IRF7是circUsp32 的下游靶点,并且直接调控巨噬细胞极化。越来越多的证据表明,CircRNAs可以与蛋白质相互作用,并参与疾病进展。为了研究CircUsp32和Socs1之间的潜在相互作用,作者进行了RNA down和RNA免疫沉淀实验,结果发现Socs1显著富集了circUsp32,CircUsp32通过竞争性结合SOCS1的SH2结构域来抑制IRF7泛素化,从而增强IRF7的表达并调节下游信号通路。为了研究CircUsp32是如何调节巨噬细胞的极化,作者进行了拯救实验,结果发现过表达circUsp32 可上调 IRF7 表达并促进促炎极化,敲低 circUsp32 可下调 IRF7 表达并抑制促炎极化,qRT-PCR 和流式细胞术进一步验证Socs1可阻断 circUsp32 对巨噬细胞炎症因子表达和极化比例的调控;证实circUsp32 通过 Socs1/IRF7轴调控巨噬细胞极化。为了评估CircUsp32在体内的作用,作者通过腺相关病毒(AAV)在小鼠脑内敲低circUsp32,分离得到TBI-EVssh-circUsp32,注射后与TBI-EVs组相比,AKI标志物显著降低,肾组织损伤缓解,巨噬细胞极化逆转,IRF7表达下调。这些发现表明,敲低circUsp32通过减少小鼠促炎巨噬细胞极化,改善了TBI诱导的AKI。作者对200例TBI患者的血浆样本分析发现,hsa_circ_0044940 与小鼠 circUsp32 序列同源性最高,AKI的患者血浆EVs中同源环状RNA hsa_circ_0044940表达显著升高,且与肾损伤标志物KIM-1和NGAL呈正相关,ROC曲线分析显示其AUC值为0.726,证实hsa_circ_0044940可作为TBI后AKI的潜在血浆EVs生物标志物。最后作者初步验证了脑与肾脏之间的双向交互作用,TBI-EVs处理可显著下调小鼠肾脏Oat1表达,导致血液中硫酸吲哚酚(IS)水平显著升高,IS蓄积引发血脑屏障(BBB)功能障碍,进而诱导神经炎症和氧化应激;敲低 circUsp32可部分恢复Oat1表达,降低血液中IS水平。
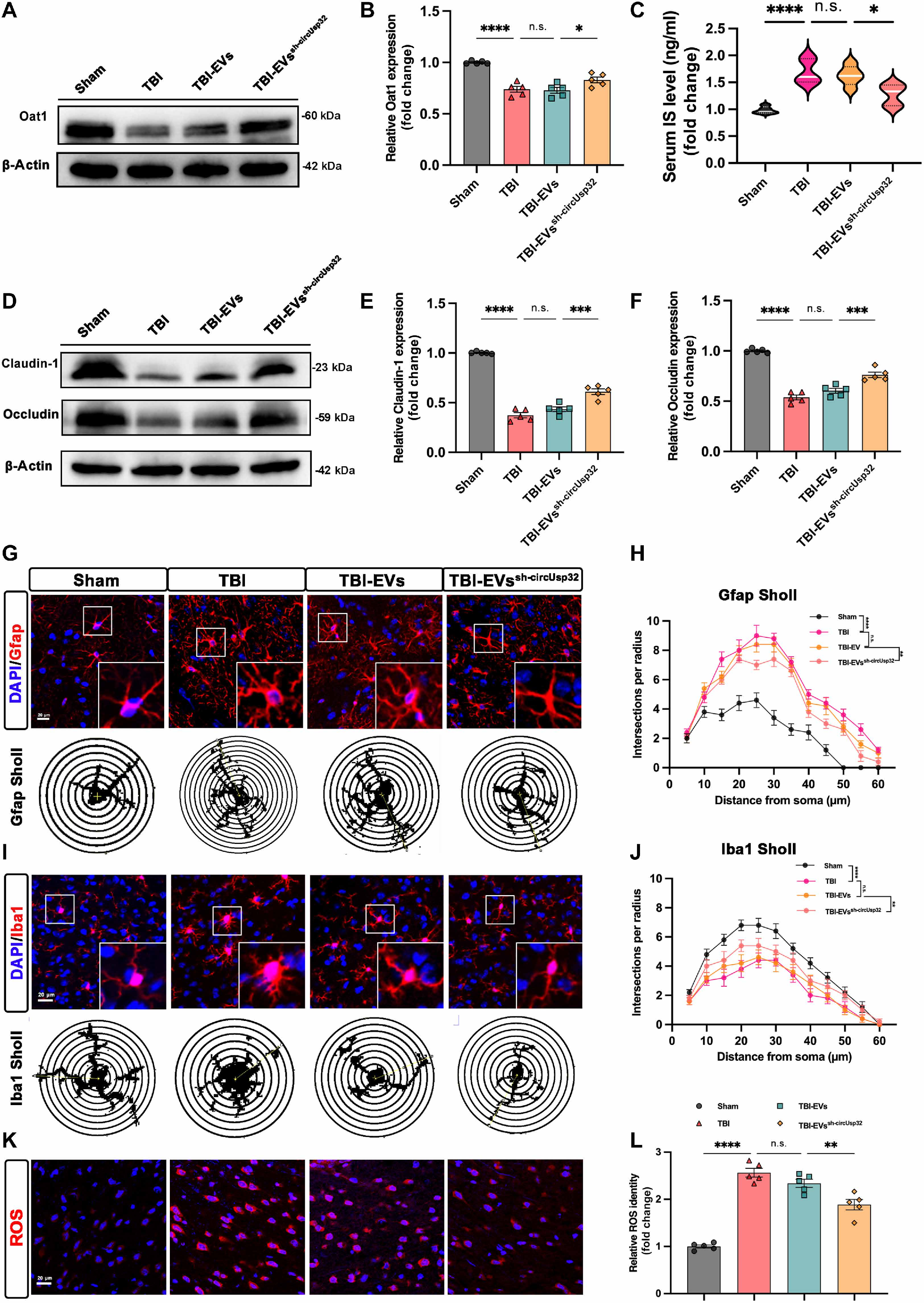
综上所述,作者认为circUsp32是TBI-EVs介导AKI的关键分子,通过Socs1/IRF7轴促进巨噬细胞促炎极化,从而引发TBI后AKI。其人类同源物hsa_circ_0044940 可作为 TBI 后 AKI 的潜在标志物,敲低circUsp32 是TBI 相关AKI的潜在治疗策略。该研究不仅深化了对TBI 后多器官损伤分子机制的理解,也为TBI 相关AKI的早期诊断和靶向治疗提供了新的实验依据和研究方向。

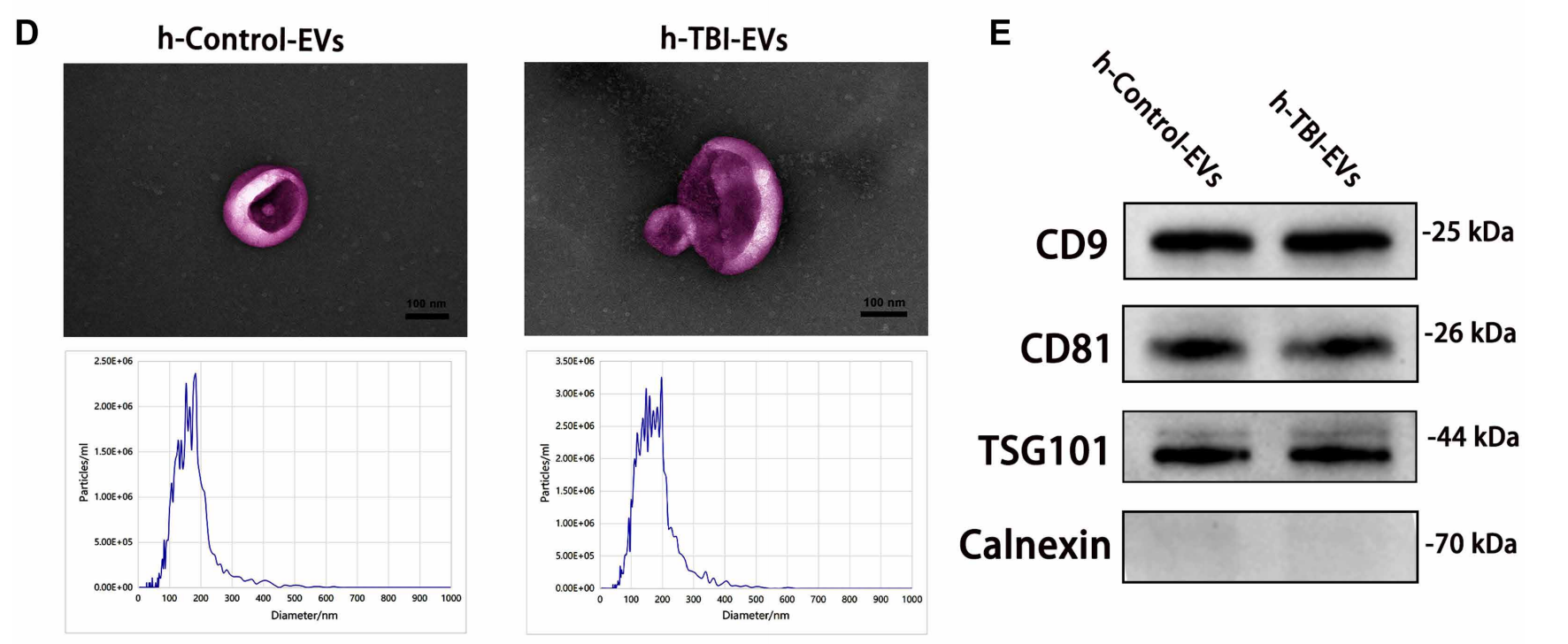
该研究中使用本公司的血清血浆外泌体提取纯化试剂盒升级版(货号:UR52151)对TBI患者和对照组血浆来源的外泌体(EVs)进行了提取纯化,随后使用外泌体蛋白专用裂解液(货号:UR33101)对外泌体进行了裂解,结果符合各检测指标要求,满足了客户下游实验需求。
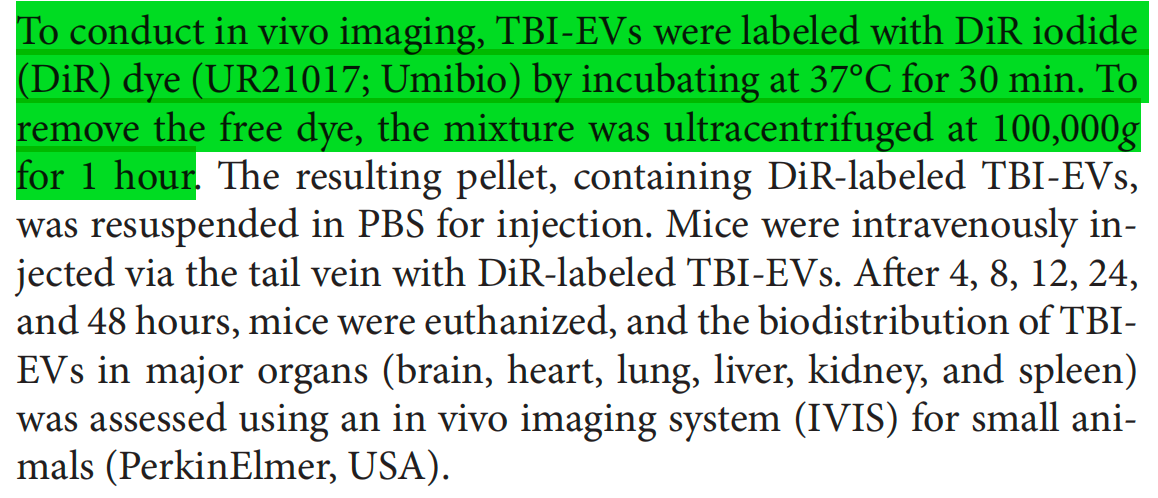
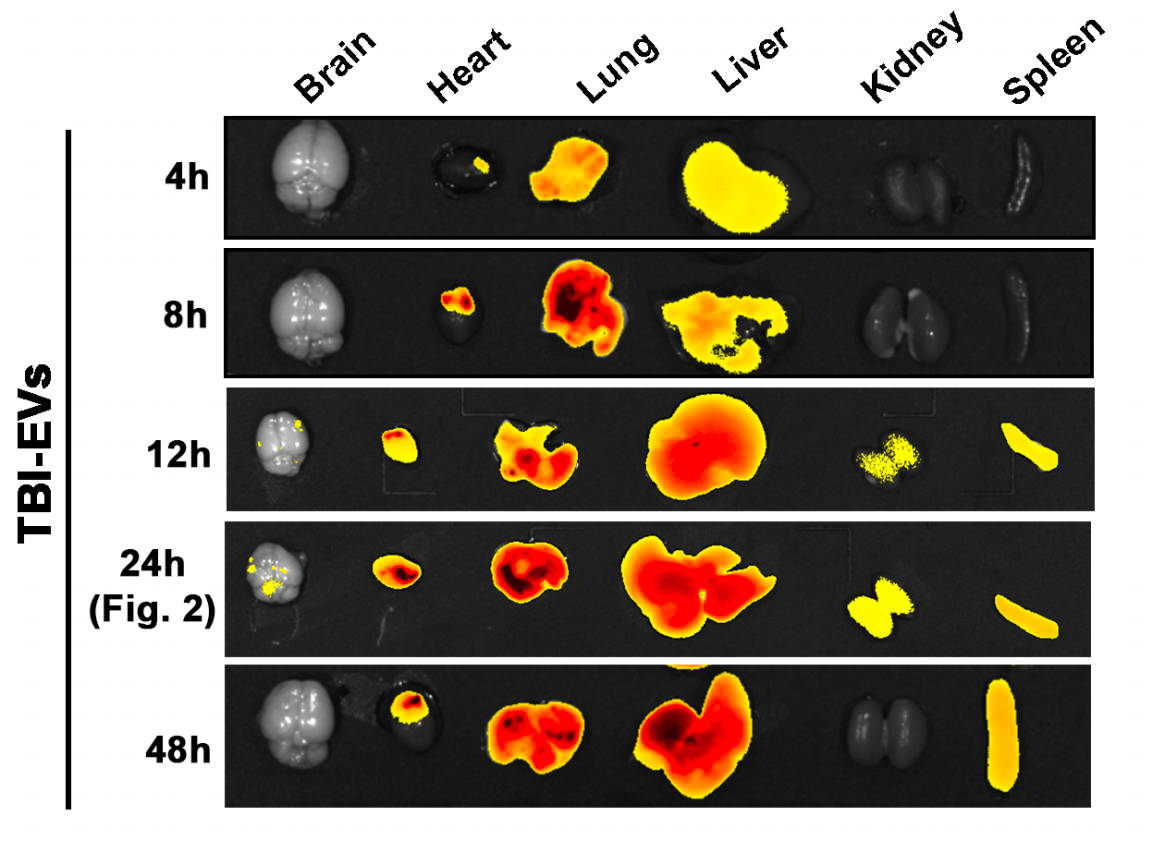
该研究中使用本公司的外泌体荧光染料DIR(货号:UR21017)对小鼠脑组织来源的外泌体(TBI-EVs)进行标记,在4、8、12、24和48小时后,利用体内成像系统(IVIS)观察了TBI-EVs在主要器官的生物分布,结果发现TBI-EVs在心脏、肺、肝、肾和脾均有分布,而脑部积累极少;TBI-EVs在肾脏中12h 达峰,48h开始下降。

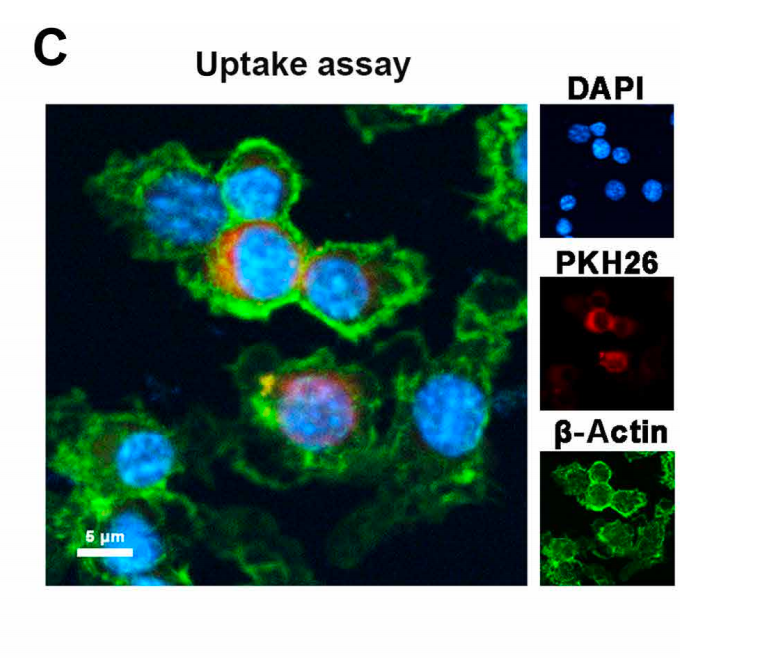
该研究中使用本公司的外泌体红色荧光标记染料(货号:UR52302)对小鼠脑组织来源的外泌体(TBI-EVs)进行标记,然后将RAW 264.7巨噬细胞与PKH26标记的TBI-EVs共孵育3小时,结果发现TBI-EVs能够被RAW 264.7巨噬细胞成功摄取。
参考文献:Brain-derived extracellular vesicles circUsp32 polarized macrophages causing acute kidney injury after traumatic brain injury.Science Advances.2025 Nov 28;11(48):eadz1243.
获取全文请扫描下方二维码: