上海宇玫博生物科技有限公司品牌商
8 年
手机商铺
- NaN
- 0.9000000000000004
- 0.9000000000000004
- 1.9000000000000004
- 0.9000000000000004
上海宇玫博生物科技有限公司
入驻年限:8 年
- 联系人:
宇玫博
- 所在地区:
上海 浦东新区
- 业务范围:
技术服务、耗材、实验室仪器 / 设备、细胞库 / 细胞培养、论文服务、试剂、原辅料包材
- 经营模式:
生产厂商 经销商 科研机构
推荐产品
公司新闻/正文
Vessel Plus 细胞外囊泡在血管疾病中的病理机制和治疗应用进展
16 人阅读发布时间:2025-12-09 14:00

近期,来自河南医药大学健康中原研究院的韩涛教授团队和上海宇玫博生物科技有限公司的高博博士在Vessel Plus杂志发表了题为“Extracellular vesicles in vascular diseases: pathological mechanisms and therapeutic application progress”的综述论文。该论文系统总结了EVs在血管疾病中的双重角色:既是病理机制中的关键介质,也是潜在的治疗工具。随着EVs工程化技术的发展和临床研究的深入,EVs有望成为血管疾病精准诊断和治疗的新一代药物。

文章导读
心血管疾病是全球死亡的主要原因,其中血管疾病以循环系统结构和功能异常为特征,会导致运动耐受度降低和多器官缺血损伤。主要的血管疾病包括动脉粥样硬化、原发性高血压、肺动脉高压、主动脉夹层和动脉瘤,它们具有共同的病理机制:内皮功能障碍或自身免疫损伤引发炎症与氧化应激导致血管平滑肌细胞异常活化或表型转换,进而引发细胞外基质失衡,最后导致病理性血管重塑。本综述聚焦这四类血管疾病作为经典案例研究,阐明细胞外囊泡(EVs)在血管病理生理中的多方面作用,新的证据表明,自身免疫介导的血管壁损伤会加剧部分患者中这些常见的致病途径。EVs 是由细胞释放的纳米级脂质双层囊泡,携带蛋白质、核酸(miRNA、mRNA、siRNA)和脂质等生物活性分子。它具有生物相容性高、免疫原性低、组织穿透性强等优势,不仅是信号传递载体(细胞因子、自身抗原、蛋白酶和miRNA),而且可以调节免疫稳态(miRNA转运蛋白和功能性蛋白,这些分子可以直接激活受体细胞中的信号通路,从而驱动血管的致病机制和修复过程);还可以作为靶向治疗递送平台。本综述阐明了EVs在血管疾病治疗中的机制作用,探索了目前增强其治疗潜力的工程化策略,并讨论了其临床转化面临的挑战和未来前景。
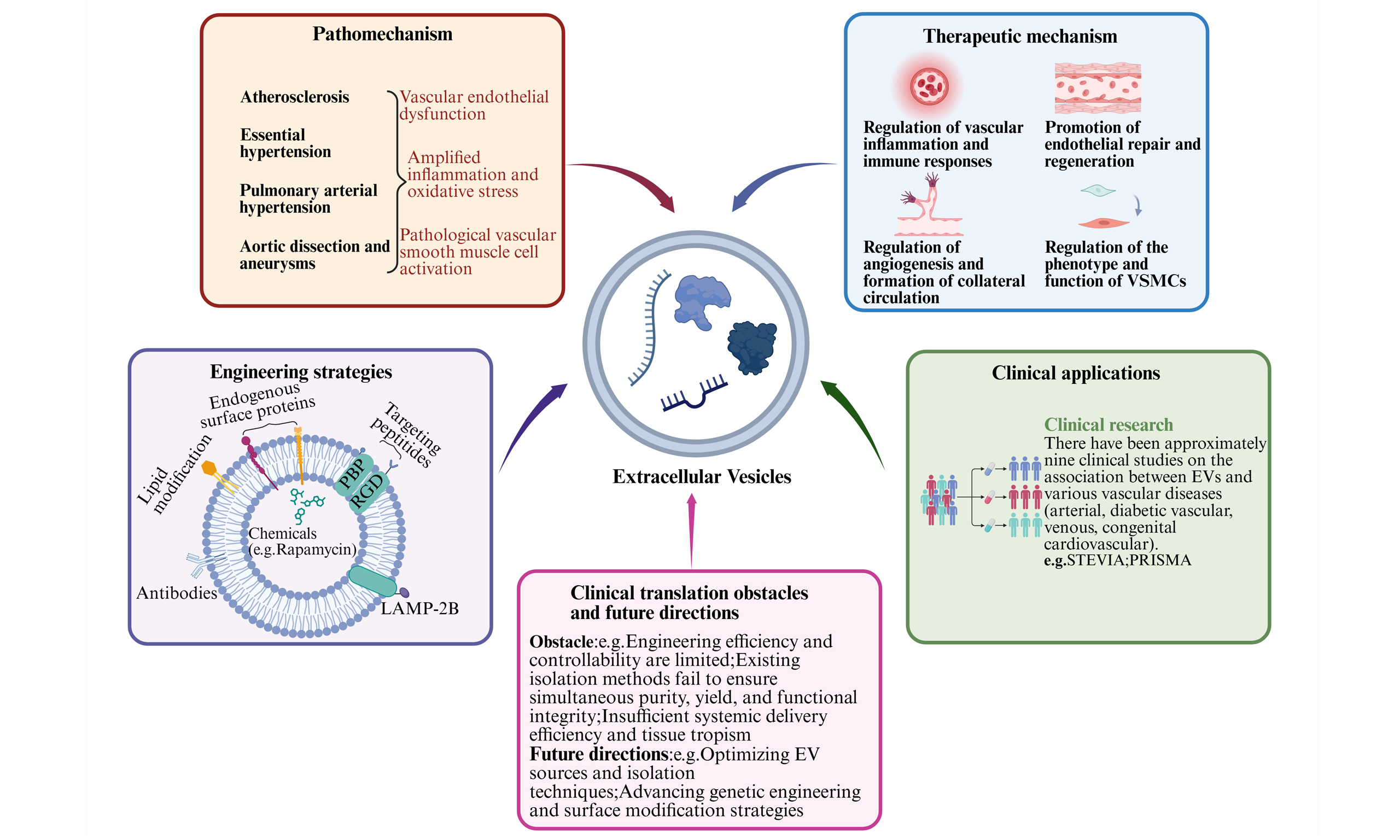
正文简介
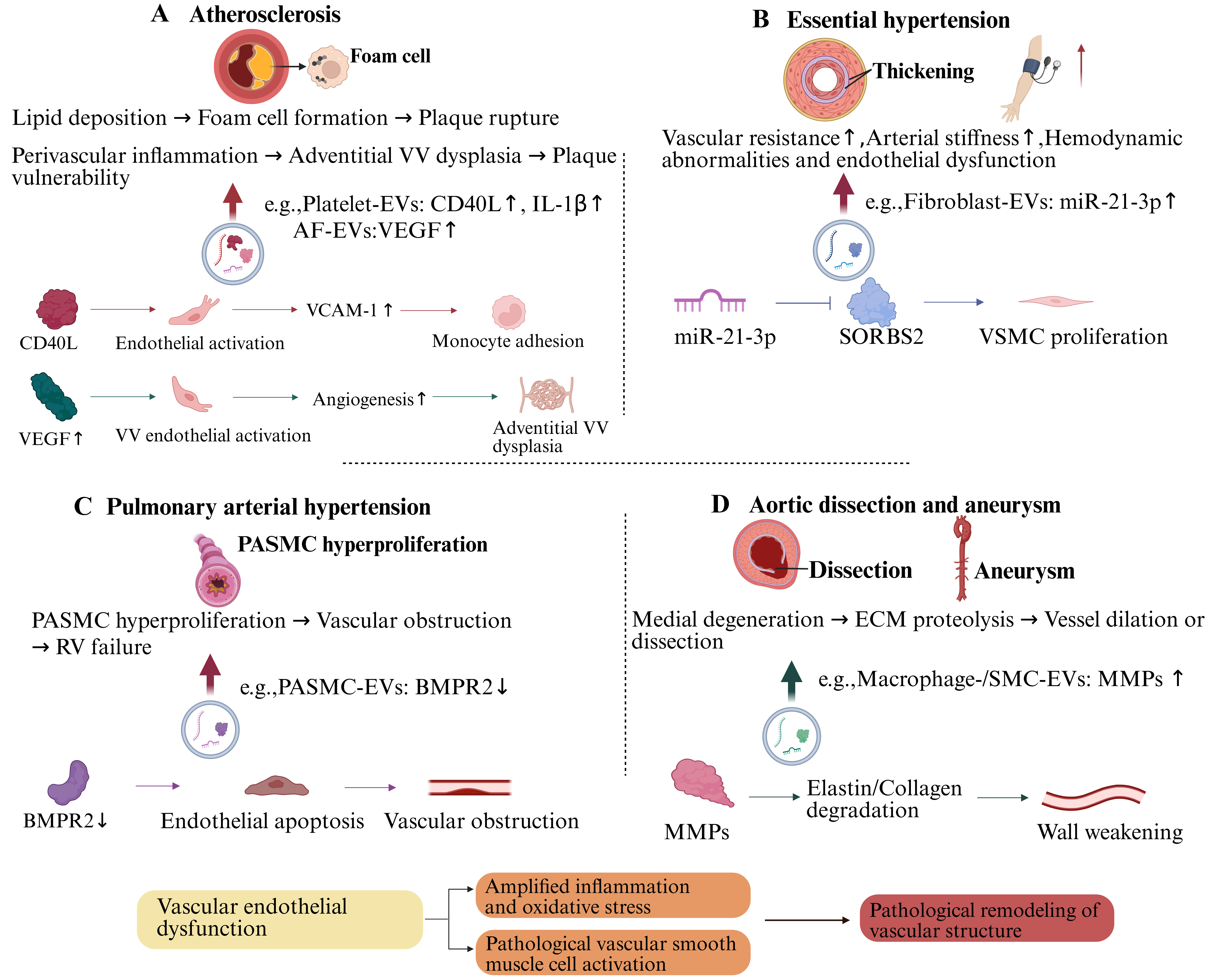
本文以四类典型血管疾病为例,阐明了EVs如何参与病理过程。动脉粥样硬化是血小板来源的EVs 携带 CD40L、IL-1β,促进内皮激活和单核细胞黏附;或是外膜成纤维细胞来源的EVs 携带血管内皮生长因子(VEGF),诱导病理性血管新生,增加斑块不稳定性。原发性高血压是成纤维细胞来源的 EVs 携带miR-21-3p,抑制SORBS2,促进血管平滑肌细胞(VSMC)增殖和血管壁增厚。肺动脉高压是肺动脉平滑肌细胞(PASMC)来源的 EVs 中BMPR2表达下降,促进内皮凋亡和PASMC过度增殖。主动脉夹层与动脉瘤是巨噬细胞和平滑肌细胞(SMC)来源的EVs携带基质金属蛋白酶(MMPs),降解细胞外基质,导致血管壁弱化。除了这些疾病特有的触发因素外,自身免疫介导的损伤在血管范围内引发或加剧这些病理性级联反应。它的核心途径是首先自身抗原的增加,然后是T细胞和B细胞的激活,最终导致炎症的放大,这一过程通常由血管自身抗原的暴露启动,并通过EV介导的沟通而被放大,导致持续的炎症和细胞功能障碍。EVs 的作用表明,它们不仅是病理信号的传递者,也是血管疾病发展中的执行者。
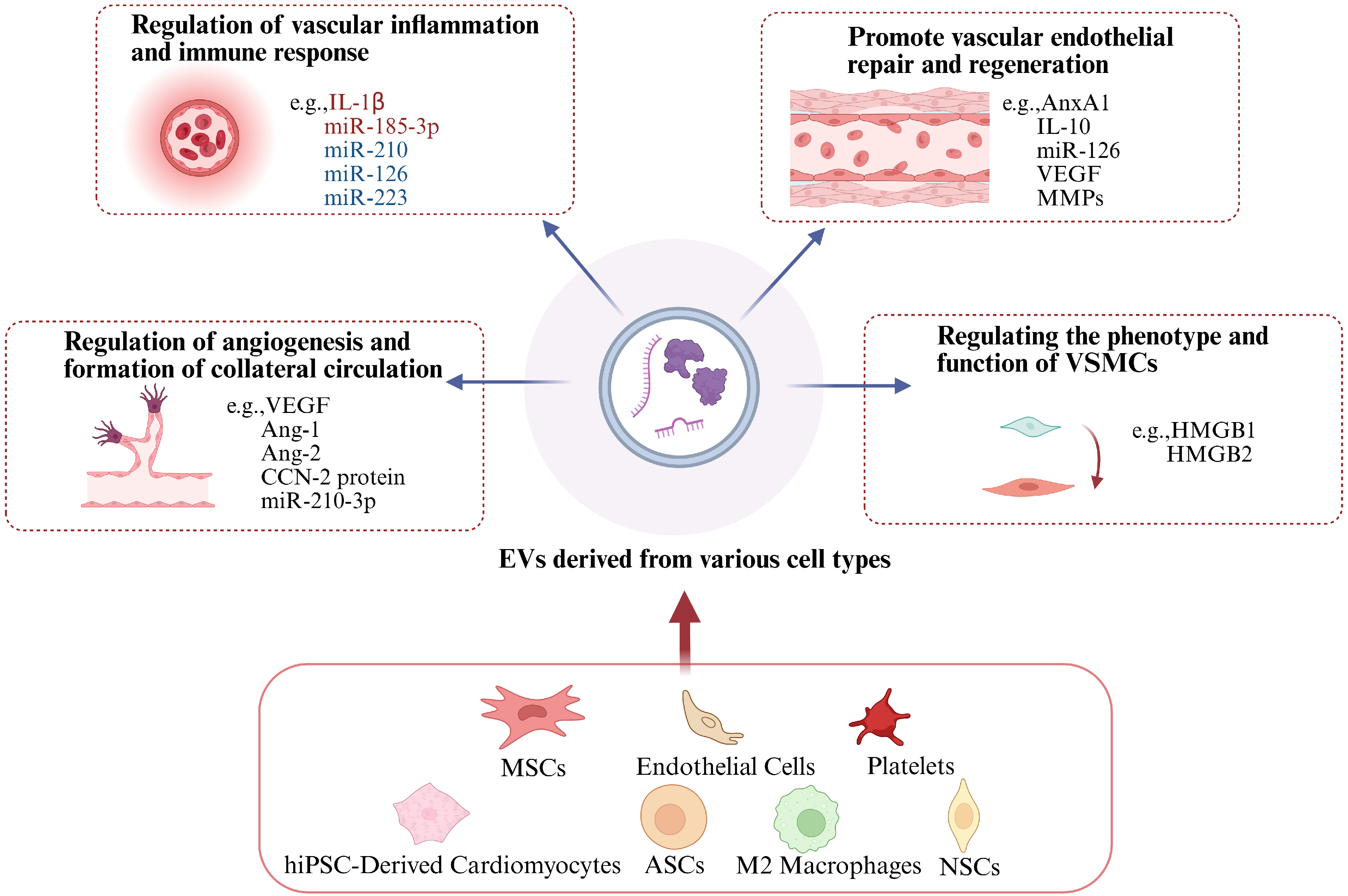
细胞外囊泡(EVs)在血管疾病治疗中展现出多方面的核心作用,它们通过递送抗炎因子、促修复分子等生物活性分子,能够精确调控血管炎症、促进内皮细胞修复与再生、诱导功能性血管新生与侧支循环建立,并调节血管平滑肌细胞的表型与功能,从而协同作用于血管稳态的恢复。具体是通过以下四个功能轴调控血管稳态:第一调节血管炎症与免疫反应,EVs 含有 IL-1β、miR-185-3p、miR-210、miR-126 和miR-223 等分子,这些物质通过调节免疫细胞(巨噬细胞、T细胞)的激活状态或血管内皮细胞分泌炎症因子,抑制过度的血管炎症反应并维持免疫稳态。第二促进血管内皮修复与再生,EVs携带ANXA1、IL-10、miR-126、VEGF和MMP等分子,这些物质调节内皮细胞增殖、迁移和损伤修复,直接促进血管内皮的修复和再生,并保持内皮屏障的完整性。第三调控血管新生与侧支循环形成,EVs传递VEGF、Ang-1、Ang-2、CCN-2蛋白和miR-210-3p等分子,这些物质作用于血管内皮细胞或周细胞,调节血管生成的内皮出芽或管腔形成,并诱导侧支循环的建立,从而改善缺血组织的血液供应。 第四调节VSMC表型与功能,EVs传递高迁移率分子组HMGB1和 HMGB2,这些物质控制血管平滑肌细胞的表型转变,并影响其增殖、迁移和分泌细胞外基质的能力,从而参与血管张力调节和血管重塑过程。EVs在血管病理表现出复杂的双重调控特性,它们既可以促进异常VSMC活化和表型转换,又可以维持内皮稳态和抑制炎症反应发挥血管保护作用。这一功能双重性表明基于不同血管病变分子特征开发特定的基于EVs的干预策略,精确调控EVs生物发生或对其分子货物的工程修饰,能够针对血管疾病进展进行靶向干预,为开发下一代血管治疗提供创新途径。
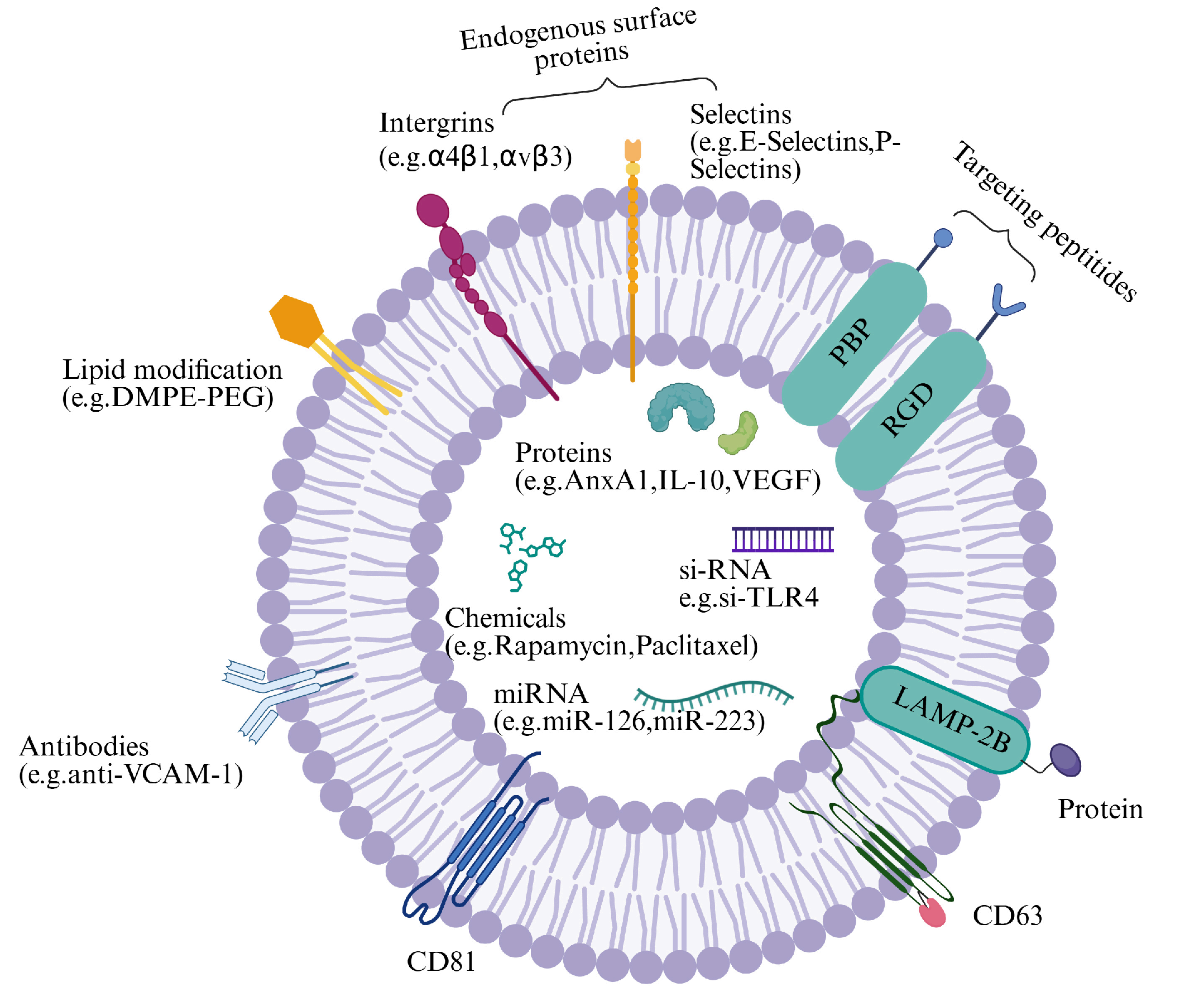
EVs在血管病理方面具有明显的治疗优势,生物相容性高、免疫原性低,可穿越血脑屏障和来源多样(干细胞来源的有ASC-EVs、BMSC-EVs、UC-MSC-EVs、iPSC-EVs和DPSC-EVs,还有血清来源的EVs)。随着EVs在治疗领域的发展,不仅有天然的EVs,还可以通过工程化改造(内容物装载和靶向肽修饰),为特定血管病变提供更强的靶向和效力,工程化EVs已在SER-VES-HEAL等临床试验中展示出促进血管修复的潜力。工程化策略通过供体细胞的基因改造、结合Lamp2b融合靶向肽、刺激响应生物材料或纳米载体的功能化实现缓释,这些综合策略共同提升了工程化EVs治疗在血管病理中的精准性和临床可行性。此外,循环 EVs中的生物标志物还可用于早期疾病诊断和预后评估,显示出诊疗一体化的应用潜力。由此可见,EVs在血管疾病中的研究不仅加深了对病理机制的理解,也为创新疗法提供了新的研究方向。
结论与展望
本综述系统阐述了细胞外囊泡在血管疾病中的双重角色:一方面,它们作为关键的病理信使,通过传递蛋白质、核酸等活性物质,驱动血管炎症、内皮损伤和平滑肌细胞异常活化等核心病变过程;另一方面,它们凭借其天然的生物相容性、低免疫原性和靶向递送能力,成为极具前景的治疗工具。通过工程化改造装载特定药物或功能性分子,EVs能够精准干预疾病进程,促进血管修复与再生。尽管在标准化生产、工程化效率、靶向精准度、系统性解析EVs功能、临床转化和精准医疗方面仍面临挑战,但EVs无疑为下一代血管疾病的精准诊断与治疗开辟了革命性的新策略。
参考文献:Extracellular vesicles in vascular diseases: pathological mechanisms and therapeutic application progress. Vessel Plus. 2025;9:21
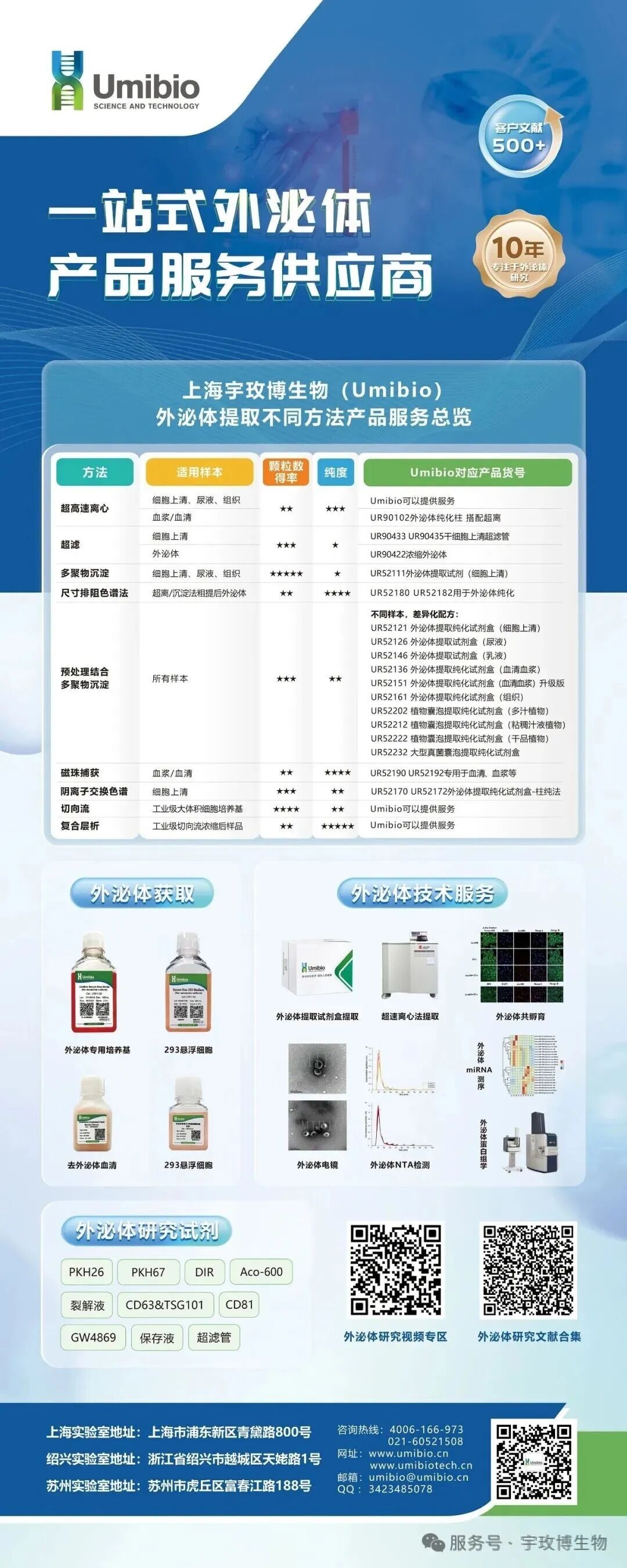
相关产品服务:https://umibio.biomart.cn
获取全文请扫描下方二维码: