上海宇玫博生物科技有限公司品牌商
8 年
手机商铺
- NaN
- 0.9000000000000004
- 0.9000000000000004
- 1.9000000000000004
- 0.9000000000000004
上海宇玫博生物科技有限公司
入驻年限:8 年
- 联系人:
宇玫博
- 所在地区:
上海 浦东新区
- 业务范围:
技术服务、耗材、实验室仪器 / 设备、细胞库 / 细胞培养、论文服务、试剂、原辅料包材
- 经营模式:
生产厂商 经销商 科研机构
推荐产品
公司新闻/正文
IF=12.6 | Umibio外泌体红色荧光标记染料助力客户紫外线诱导的皮肤损伤研究!
65 人阅读发布时间:2025-12-01 20:36

近期,来自第四军医大学西京医院的坚哲教授和李春英教授团队在Journal of Nanobiotechnology杂志发表了题为“Microneedles combining delivery of hUMSC-derived exosomes and EGCG mitigate UV-induced skin damage”的科研论文,IF=12.6。

研究背景:
紫外线(UVB,290–320 nm)暴露会导致皮肤氧化应激、炎症、DNA损伤、细胞膜破坏、细胞坏死或凋亡,传统治疗方法如非甾体抗炎药和防晒霜效果有限,且无法逆转累积性损伤和慢性病理影响。间充质干细胞衍生的外泌体 (MSCExo) 作为细胞间通讯的关键介质,富含多种生物活性分子,包括蛋白质、脂质和核酸。人脐带源性间充质外泌体(hUMSC-Exo)具有强大的抗炎、促进组织再生和免疫调节功能。然而与传统抗氧化剂相比,hUMSC-Exo间接中和自由基和减轻氧化应激的能力有限。亲脂性EGCG是一种来自绿茶的天然多酚,具有强大的抗氧化特性,并能有效抵消紫外线诱导的细胞和组织氧化损伤。两者理论上有协同效应,但都面临皮肤渗透性差、稳定性低、体内半衰期短的递送挑战。因此,开发一种能够突破皮肤屏障、实现高效共递送的新型策略,成为解决这一临床挑战的迫切需求。微针技术可以直接、微创、无痛地通过角质层给药,研究表明微针技术可以克服hUMSC-Exo和EGCG的递送限制,增强它们在紫外线损伤皮肤中的保留和治疗性能。本文作者开发了一种由HAMA/PVA基质组成的可溶性微针,旨在减轻紫外线诱导的皮肤损伤。
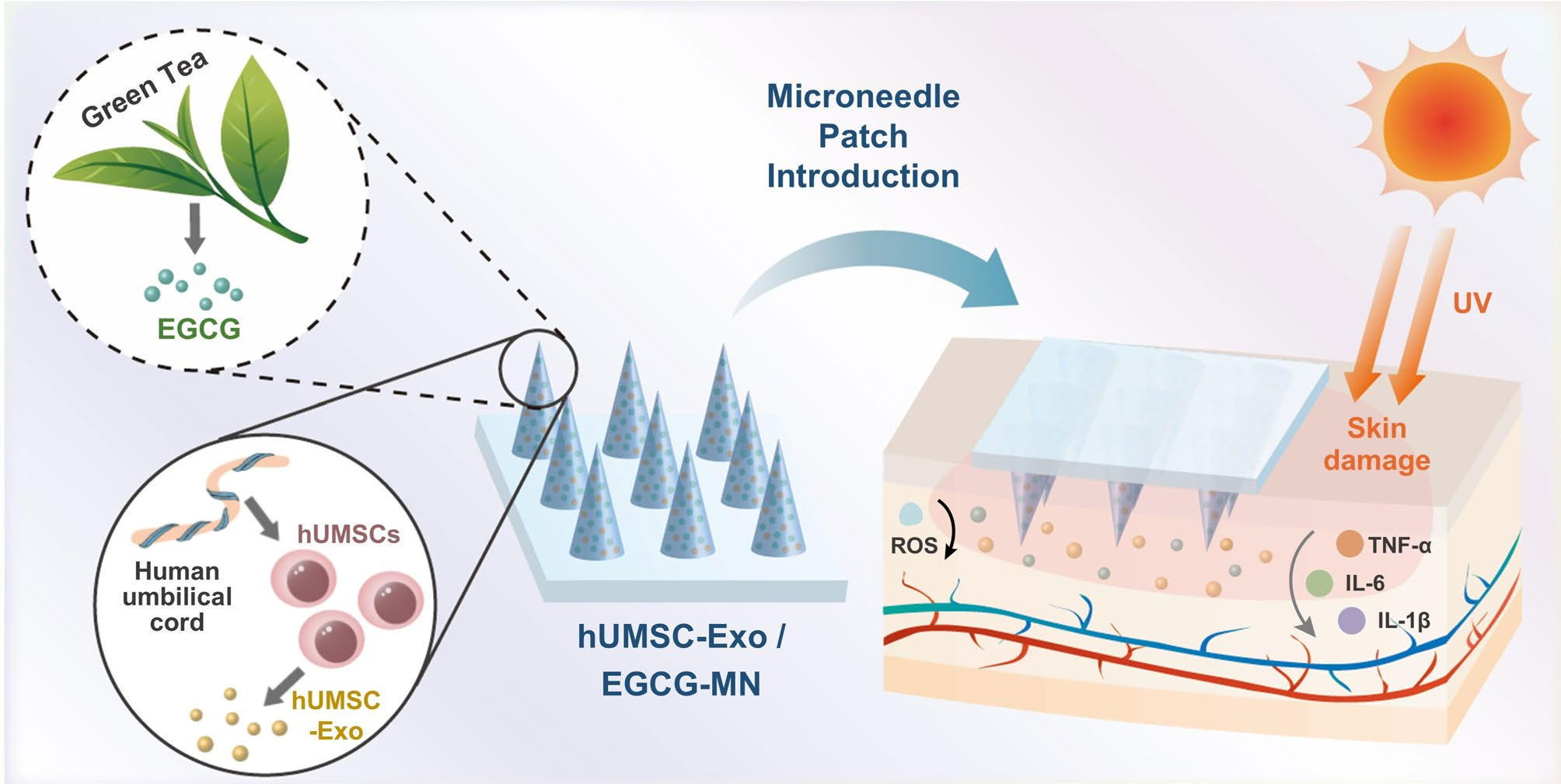
研究成果及意义:
在本研究中,作者首先通过超速离心法从人脐带间充质干细胞上清液中提取出外泌体并进行了表征和细胞摄取。结果显示提取的外泌体颗粒大小为119 nm左右,典型的茶托形态,并表达外泌体阳性标志物(CD9, TSG101, Alix),不表达阴性标志物(Calnexin),同时该外泌体能被HaCaT细胞成功摄取。接着作者进行了hUMSC-Exo和EGCG 对 HaCaT细胞的生物相容性测试,结果发现hUMSCExo 和 EGCG 均表现出优异的生物相容性,并且hUMSC-Exo/EGCG的协同作用显著增强了HaCaT细胞增殖。而后作者构建了体外氧化应激模型来评估hUMSC-Exo/EGCG的抗氧化能力、抗DNA损伤和抗炎效果。结果发现hUMSC-Exo和EGCG的协同使用在清除ROS和总抗氧化能力上表现最好,效果优于单一成分;它们的协同使用能最有效地减少UVB诱导的γ-H2AX含量,并且能最显著地降低HaCaT细胞分泌的TNF-α, IL-6, IL-1β表达水平。这表明hUMSC-Exo/EGCG 组合可以优势互补,协同增强抗氧化、抗DNA损伤和抗炎特性。体外细胞实验证明了hUMSC-Exo/EGCG 具有强大的抗氧化和抗炎作用,然而其在体内的应用因透皮性能差而受到严重阻碍。微针(MN)优异的透皮性能使它们能够有效和快速地通过皮肤层输送药物,于是作者开发了一种装载hUMSC-Exo/EGCG的微针(hUMSC-Exo/EGCG-MN)来增强 hUMSC-Exo/EGCG 的功效并延长其组织递送的持续时间。随后对其进行了性能测试,扫描电镜结果显示微针阵列排列整齐,结构完整;CCK-8和活/死细胞染色表明,hUMSC-Exo/EGCG-MN具有良好的生物相容性,并且不会对细胞造成损伤;质地分析仪测试表明,微针能承受≥1.4 N的力,远高于皮肤穿刺所需的最小力(0.058 N),hUMSC-Exo/EGCG-MN具有足够的机械强度来穿透皮肤;H&E染色和亚甲基蓝染色证实hUMSC-Exo/EGCG-MN能有效刺穿过角质层进入真皮层形成微孔,且孔道在30分钟内自行闭合;在PBS中模拟释放证明了EGCG和hUMSC-Exo能从微针中持续释放,且释放后的外泌体仍保持结构完整。为了研究hUMSC-Exo/EGCG-MN对紫外线诱导的BALB/c小鼠皮肤损伤的治疗作用,作者构建了紫外线诱导的BALB/c小鼠皮肤损伤模型,并进行H&E染色和免疫组织化学染色实验。结果表明 hUMSC-Exo/EGCG-MN可减轻紫外线引起的小鼠皮肤组织学损伤,促进胶原蛋白沉积,并避免光老化。随后作者又进行了Ki67染色,免疫荧光染色和免疫组织化学染色等实验,结果与体外细胞实验的结果一致,表明hUMSC-Exo/EGCG-MN可以减少氧化损伤,增加抗氧化活性,并改善紫外线照射引起的皮肤炎症。最后,作者进行了RNA测序分析来深入研究hUMSC-Exo/EGCG-MN减轻UVB诱导损伤的作用机制。结果发现治疗组与对照组之间存在1384个差异表达基因,其中683个基因下调,701个基因上调;KEGG分析显示hUMSC-Exo/EGCG-MN治疗激活了内吞作用、AMPK、PI3K-Akt、JAK-STAT等与细胞存活、增殖、代谢和抗炎相关的通路,同时抑制了细胞凋亡、衰老等相关通路。这表明hUMSC-Exo/EGCG-MN 通过激活多种信号通路促进细胞存活、增殖、能量稳态和新血管形成,从而支持细胞对损伤的修复反应并增强组织再生。为了阐明 hUMSCExo/EGCG 抑制光损伤的具体机制,作者从小鼠皮肤的RNA测序分析中筛选了12个DEGs,并在HaCaT细胞中进行了体外验证。结果发现hUMSC-Exo/EGCG能显著下调IL-1β 和上调SOD2。为了进一步研究这些靶标的功能作用,在Exo/EGCG 存在的情况下,作者重组了 IL-1β 蛋白和 2-甲氧基雌二醇。功能实验表明人为激活IL-1β或抑制SOD2都会逆转hUMSC-Exo/EGCG的保护作用,从而导致ROS、DNA损伤和炎症因子水平回升,其中IL-1β的激活可能在调控途径中发挥了更关键的作用。上述结果表明抑制 IL-1β 和激活 SOD2 是 hUMSC-Exo/EGCG 减轻UVB诱导的皮肤光损伤的关键机制。
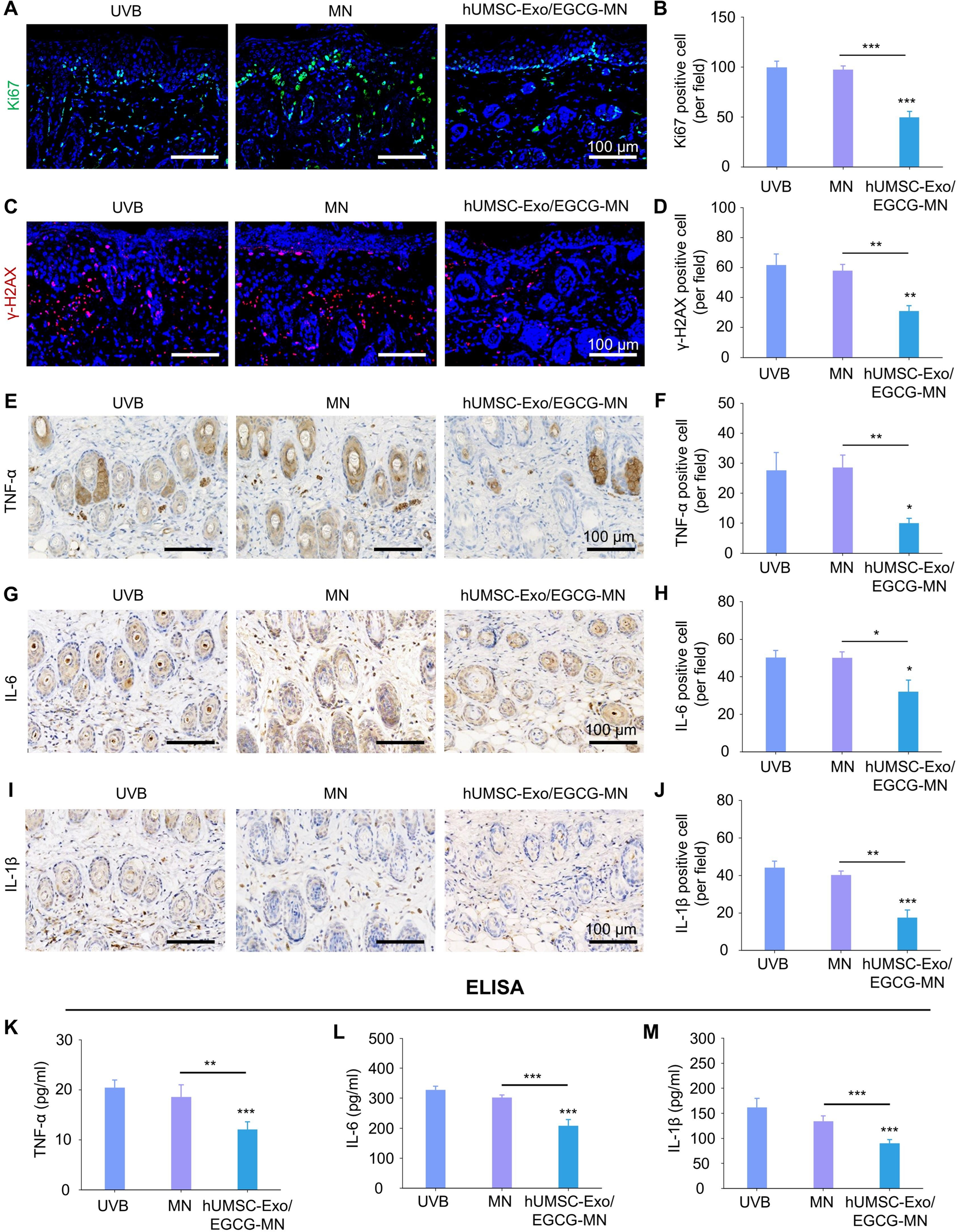
综上所述,作者成功开发了一种负载人脐带间充质干细胞外泌体(hUMSC-Exo)与表没食子儿茶素没食子酸酯(EGCG)的可溶性微针贴片。该微针贴片通过高效穿透皮肤屏障,实现了两种活性成分的协同递送,在细胞和动物模型中均被证实能显著修复紫外线诱导的皮肤损伤,其核心机制在于通过抑制IL-1β和激活SOD2的双重调控机制,从而在多维度上协同发挥抗炎、抗氧化及促进组织再生的卓越疗效,为皮肤光损伤治疗提供了一种兼具创新性与临床应用前景的新策略。

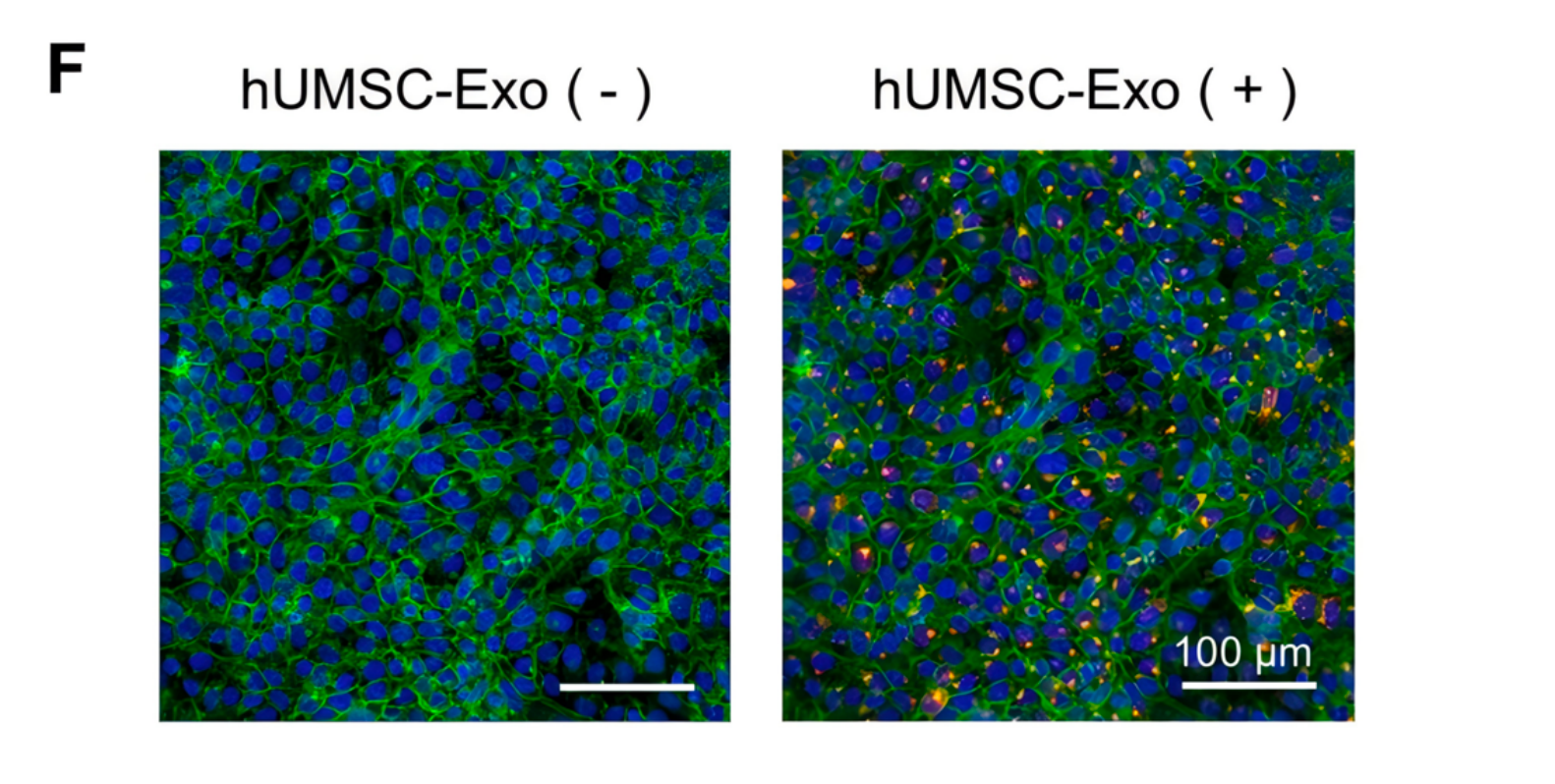
该研究中使用本公司的外泌体红色荧光标记染料(货号:UR52302)对人脐带间充质干细胞来源的外泌体(hUMSC-Exo)进行标记,然后将HaCaT细胞与PKH26标记的外泌体共孵育12小时,结果发现人脐带间充质干细胞来源的外泌体(hUMSC-Exo)能够被HaCaT细胞成功摄取。本公司开发了人脐带间充质干细胞来源的外泌体(MSC-Exo)(货号:UR53233)供科研客户使用。
参考文献:
Microneedles combining delivery of hUMSC-derived exosomes and EGCG mitigate UV-induced skin damage. Journal of Nanobiotechnology. 2025 Oct 10;23(1):643.
相关产品:
获取全文请扫描下方二维码: